Einführung in die Qualifizierung
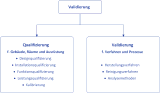
Die Qualifizierung ist Teil der Validierung und umfasst alle Maßnahmen, mit Hilfe derer nachgewiesen und dokumentiert wird, dass sämtliche die Produktqualität beeinflussenden Räumlichkeiten, Ausrüstungen oder Hilfssysteme
- sachgemäß angelegt oder installiert sind
- ordnungsgemäß funktionieren und
- tatsächlich zu den erwarteten Ergebnissen führen
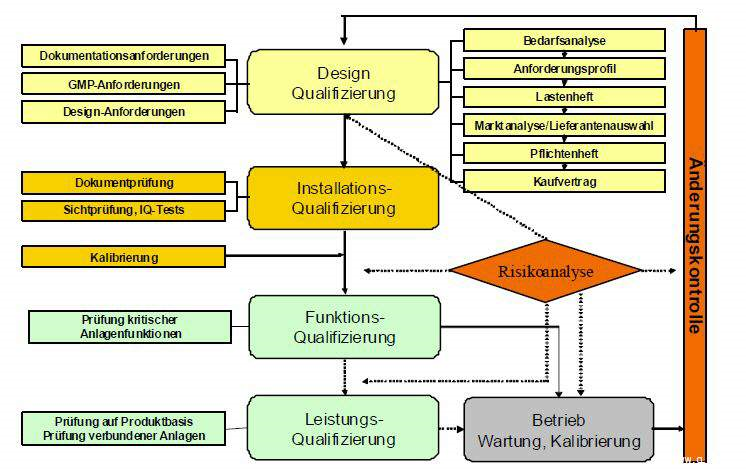
Qualifizierung ist ein mehrstufiger Prozess und umfasst
- die Designqualifizierung (DQ)
- die Installationsqualifizierung (IQ)
- die Funktionsqualifizierung (OQ) und
- die Leistungsqualifizierung (PQ).
Die Ergebnisse werden im Qualifizierungsbericht festgehalten. Dieser wird den Auditoren und Kunden als Nachweis vorgelegt.
Was wird Qualifiziert? | Was wird Validiert?
Kurz gesagt ...
Geräte werden qualifiziert
Prozesse werden validiert
Die Umfänge und Tiefe der Validierungsaktivitäten sind mittels einer Risikobewertung festzulegen. Ebenso werden die relevanten Geräte und Gewerke zum Beispiel über ein Risk-Assessment identifiziert.
Ihre Experten für GMP-konforme Qualifizierung und Validierung
CLS unterstützt Sie in allen Phasen der Qualifizierung und Validierung. Oftmalige Durchführung und langjährige Erfahrungen garantieren effiziente Umsetzung und ansprechende Qualität.